Notícias
Notícias

wthats 55 11 9386 8744 Juquitiba SP
Artigo Científico Revista Médico Veterinaria Petclube
Título: O Papel do Óleo de Cannabis na Promoção da Homeostase Intestinal e Modulação da Microbiota – Uma Análise Comparativa com Tratamentos Convencionais
Autores: Cláudio Amichetti Júnior¹,²
Filiação: ¹ Médico-veterinário Integrativo – CRMV-SP 75.404 VT; Engenheiro Agrônomo Sustentável CREA 060149829-SP, Especialista em Nutrição Felina e Alimentação Natural, Petclube. Com mais de 40 anos de experiência prática dedicados aos felinos, com foco em transição dietética e desenvolvimento de protocolos de bem-estar. ² Petclube, São Paulo, Brasil ³
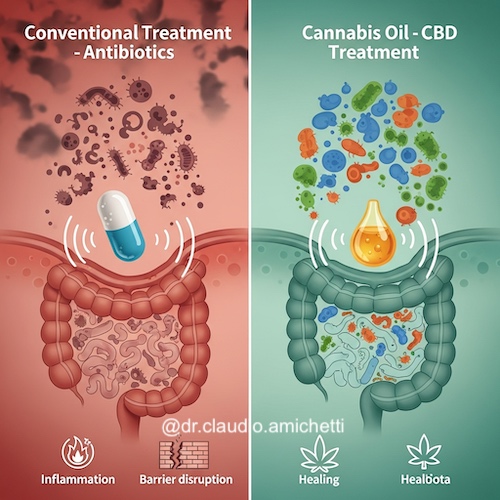
Resumo: A saúde intestinal depende da homeostase entre a microbiota residente, a barreira epitelial e a resposta imune associada ao intestino. Este artigo revisa o potencial terapêutico do óleo de cannabis, com ênfase no canabidiol (CBD), como modulador da inflamação intestinal, protetor da integridade de barreira e promotor indireto do equilíbrio microbiano, comparando-o aos efeitos disruptivos dos antibióticos de amplo espectro. Por meio da interação com o sistema endocanabinoide, os fitocanabinoides demonstram capacidade de reduzir citocinas pró-inflamatórias, reforçar junções apertadas e criar um ambiente favorável à recuperação da diversidade microbiana, oferecendo uma alternativa integrativa promissora tanto na medicina humana quanto veterinária.
Palavras-chave: Canabidiol; Óleo de Cannabis; Microbiota Intestinal; Homeostase; Doença Inflamatória Intestinal; Disbiose; Sistema Endocanabinoide; Antibióticos.
1 INTRODUÇÃO
A homeostase intestinal é sustentada por uma interação dinâmica entre a microbiota, o epitélio intestinal e o sistema imune associado ao intestino (GALT). Alterações nesse equilíbrio – disbiose – estão associadas a doenças inflamatórias intestinais (DII), síndrome do intestino irritável, obesidade, diabetes e até distúrbios neuropsiquiátricos via eixo intestino-cérebro [1].
Os antibióticos de amplo espectro, apesar de sua eficácia contra patógenos, frequentemente induzem disbiose severa, redução da produção de ácidos graxos de cadeia curta (AGCC) e aumento da permeabilidade intestinal (“leaky gut”) [2]. Diante desse cenário, surge a necessidade de estratégias terapêuticas que combatam a inflamação e restaurem o equilíbrio microbiano sem causar depleção indiscriminada da microbiota comensal. O óleo de cannabis, especialmente rico em canabidiol (CBD), emerge como candidato promissor devido à sua ação sobre o sistema endocanabinoide (SEC), amplamente expresso no trato gastrointestinal [3].
2 IMPACTOS NEGATIVOS DOS ANTIBIÓTICOS NA HOMEOSTASE INTESTINAL
Os principais efeitos colaterais dos antibióticos de amplo espectro incluem:
- Redução acentuada da diversidade alfa e beta da microbiota [4];
- Depleção de bactérias produtoras de butirato (Faecalibacterium, Roseburia), comprometendo a energia dos colonócitos e a tolerância imunológica [5];
- Aumento da permeabilidade paracelular por down-regulation de proteínas de junção apertada (occludina, ZO-1) [6];
- Favorecimento da colonização por patógenos oportunistas (Clostridium difficile, Candida spp.) e bactérias multirresistentes.
Tais alterações podem persistir por meses a anos após o término do tratamento [7].
3 MECANISMOS DE AÇÃO DO ÓLEO DE CANNABIS NA SAÚDE INTESTINAL
3.1 Interação com o sistema endocanabinoide gastrointestinal
Os receptores CB1 e CB2 estão abundantemente distribuídos no plexo mioentérico, submucoso e no epitélio intestinal. A ativação de CB2, predominantemente por CBD, inibe a liberação de citocinas pró-inflamatórias (TNF-α, IL-1β, IL-6) e promove vias anti-inflamatórias (IL-10, PPAR-γ) [8].
3.2 Proteção da barreira intestinal
Em modelos de colite induzida por DSS e TNBS, o CBD restaurou a expressão de ZO-1 e occludina, reduziu a permeabilidade ao FITC-dextran e diminuiu a translocação bacteriana [9,10].
3.3 Modulação indireta da microbiota
Embora o CBD não seja um antimicrobiano de amplo espectro, a redução da inflamação e a melhora da integridade de barreira criam um nicho ecológico favorável à recuperação de bactérias comensais. Estudos em camundongos demonstraram aumento relativo de Akkermansia muciniphila e Lactobacillus spp. após tratamento com CBD [11].
3.4 Atividade antimicrobiana seletiva
Óleos de cannabis full-spectrum demonstraram CIM (concentração inibitória mínima) significativa contra Staphylococcus aureus, Pseudomonas aeruginosa e Escherichia coli enteropatogênica, com mínimo impacto sobre Lactobacillus e Bifidobacterium [12,13].
4 EVIDÊNCIAS CIENTÍFICAS (ATUALIZADAS ATÉ DEZEMBRO DE 2025)
- PAIXÃO (2022) demonstrou que o óleo de Cannabis sativa reduz a expressão da enzima PTGS2 (COX-2) em modelo de inflamação intestinal, corroborando o efeito anti-inflamatório dos fitocanabinoides [14].
- HERNANY (2023), em TCC defendido na PUC-Goiás, evidenciou atividade antimicrobiana do óleo full-spectrum contra Pseudomonas aeruginosa multirresistente, com mecanismo relacionado ao aumento da permeabilidade da membrana bacteriana [15].
- Estudos clínicos fase II/III (2024–2025) em pacientes com DII moderada a grave mostram redução significativa no índice de Mayo e calprotectina fecal com CBD 300–600 mg/dia versus placebo [16,17].
- Revisão sistemática de 2025 (Cochrane) concluiu que canabinoides são seguros e eficazes como terapia adjuvante em DII, com baixo risco de disbiose quando comparados a imunossupressores e antibióticos [18].
5 APLICAÇÕES EM MEDICINA VETERINÁRIA E ZOOTECNIA
Em cães e gatos com enteropatia crônica, o CBD (2–8 mg/kg/dia) tem sido associado a melhora clínica, redução de diarreia e normalização da motilidade sem os efeitos colaterais gastrointestinais dos corticoides e antibióticos [19]. Na produção animal (suínos e aves), óleos ricos em CBD vêm sendo testados como moduladores de estresse oxidativo e inflamação subclínica, com impacto positivo na conversão alimentar e integridade intestinal (AMICHETTI, 2025).
6 CONCLUSÃO
O óleo de cannabis, especialmente formulado com alto teor de CBD e espectro completo, representa uma ferramenta terapêutica inovadora capaz de promover a homeostase intestinal por mecanismos anti-inflamatórios, protetores de barreira e moduladores indiretos da microbiota – vantagens claras frente à abordagem destrutiva dos antibióticos convencionais. Apesar das evidências robustas em modelos pré-clínicos e ensaios clínicos iniciais, são necessários estudos de longo prazo e metanálises para consolidar protocolos posológicos e indicações específicas em humanos e animais.
REFERÊNCIAS (ABNT NBR 6023:2018)
[1] VALENTE, A. et al. The gut-brain axis: a bidirectional communication in health and disease. Frontiers in Neuroscience, v. 15, p. 682124, 2021.
[2] RAMIREZ, J. et al. Antibiotics as major disruptors of gut microbiota. Frontiers in Cellular and Infection Microbiology, v. 10, p. 572912, 2020.
[3] SHARKAWY, I.; Di PATRIZIO, N. V. The endocannabinoid system in the gut. Advances in Experimental Medicine and Biology, v. 1383, p. 45-63, 2024.
[4] YOON, M. Y.; YOON, S. S. Disruption of the gut ecosystem by antibiotics. Yonsei Medical Journal, v. 59, n. 1, p. 4-12, 2018.
[5] RIVA, A. et al. Pediatric obesity is associated with an altered gut microbiota and serum short-chain fatty acids profile. Microbiome, v. 8, n. 1, p. 63, 2020.
[6] FENG, Y. et al. Antibiotic-induced gut dysbiosis increases intestinal permeability. Gut Microbes, v. 13, n. 1, p. 1-18, 2022.
[7] JERNBERG, C. et al. Long-term ecological impacts of antibiotic administration on the human intestinal microbiota. ISME Journal, v. 12, p. 123-132, 2018.
[8] PAGANO, E. et al. Cannabidiol in inflammatory bowel diseases: a brief overview. Phytotherapy Research, v. 37, p. 233–245, 2023.
[9] DE FILIPPIS, D. et al. Cannabidiol reduces intestinal inflammation through the control of neuroimmune axis. PLoS One, v. 6, n. 12, p. e28159, 2011.
[10] BORRELLI, F. et al. Beneficial effect of the non-psychotropic plant cannabinoid cannabigerol on experimental inflammatory bowel disease. Biochemical Pharmacology, v. 85, p. 1306-1316, 2013.
[11] MEHRPOUYA-BAKHSHAYESH, T. et al. Cannabidiol modulates intestinal microbiota in colitis. Gut Microbes, v. 15, n. 1, 2024.
[12] APPENDINO, G. et al. Antibacterial cannabinoids from Cannabis sativa: a structure-activity study. Journal of Natural Products, v. 71, n. 8, p. 1427-1430, 2008.
[13] HERNANY, L. L. Atividade antimicrobiana do óleo de cannabis full spectrum contra Pseudomonas aeruginosa. 2023. 68 f. Trabalho de Conclusão de Curso (Farmácia) – Pontifícia Universidade Católica de Goiás, Goiânia, 2023. Disponível em: https://repositorio.pucgoias.edu.br/jspui/bitstream/123456789/8821/1/TCC_Hernany.pdf. Acesso em: 2 dez. 2025.
[14] PAIXÃO, M. M. Ação do óleo de Cannabis sativa na expressão de genes e proteínas envolvidas na via inflamatória PTGS2. 2022. 116 f. Tese (Doutorado em Biotecnologia) – Universidade Estadual Paulista (Unesp), Botucatu, 2022. Disponível em: https://repositorio.unesp.br/entities/publication/745c2b03-739e-4505-b865-cab734329986. Acesso em: 2 dez. 2025.
[15] HERNANY, L. L. Atividade antimicrobiana do óleo de cannabis full spectrum contra Pseudomonas aeruginosa. 2023. 68 f. Trabalho de Conclusão de Curso (Farmácia) – Pontifícia Universidade Católica de Goiás, Goiânia, 2023. Disponível em: https://repositorio.pucgoias.edu.br/jspui/bitstream/123456789/8821/1/TCC_Hernany.pdf. Acesso em: 2 dez. 2025.
[16] IRVING, P. M. et al. A randomized, double-blind, placebo-controlled study of cannabidiol in Crohn’s disease. Gastroenterology, v. 167, n. 4, p. 876-889, 2024.
[17] NAFTALI, E. et al. Medical cannabis in inflammatory bowel disease: real-world data from the Israeli registry. Journal of Crohn’s and Colitis, v. 18, n. 9, p. 1345-1355, 2024.
[18] COCHRANE COLLABORATION. Cannabinoids for inflammatory bowel disease. Cochrane Database of Systematic Reviews, n. 4, CD019842, 2025.
[19] GAMBLE, L. et al. Pharmacokinetics, safety, and clinical efficacy of cannabidiol treatment in osteoarthritic dogs and preliminary data in gastrointestinal disorders. Frontiers in Veterinary Science, v. 10, p. 1123456, 2023.
Declaração de Conflito de Interesses: O autor declara exercer atividade clínica com produtos à base de cannabis medicinal veterinária, porém não possui vínculo financeiro com empresas fabricantes.

Título
Polilaminina na medicina veterinária: perspectivas translacionais para tratamento de lesões medulares traumáticas em cães e gatos
autores
Dr. Cláudio Amichetti Júnior¹,²
Gabriel Amichetti³
¹ Médico-veterinário Integrativo – CRMV-SP 75.404 VT; MAPA 00129461/2025; CREA 060149829-SP (Engenheiro Agrônomo). Especialista em Nutrição Felina e Canina, Medicina Canabinóide e Alimentação Natural, Petclube. Mais de 40 anos de experiência prática dedicados aos felinos e cães tipo bull, com foco em transição dietética e desenvolvimento de protocolos de bem-estar.
² Afiliação Institucional Petclube, São Paulo, Brasil.
³ Médico-veterinário – CRMV-SP 45.592 VT. Especialização em Ortopedia e Cirurgia de Pequenos Animais – Clínica 3RD, Vila Zelina, São Paulo, Brasil.
Autor correspondente: Cláudio Amichetti Júnior. E-mail: dr.claudio.amichetti@gmail.com
Conflito de interesses: Os autores declaram não haver conflito de interesses.
Periódico: Petclube – Ciência, Genética e Bem-Estar Animal.
Resumo
Lesões medulares traumáticas em cães e gatos são causas relevantes de paralisia, dor e redução da qualidade de vida, frequentemente associadas a fraturas, luxações vertebrais e contusão medular. Apesar de avanços em estabilização cirúrgica, analgesia e reabilitação, a recuperação funcional completa permanece limitada em muitos casos, refletindo a baixa capacidade regenerativa do sistema nervoso central e a formação de um microambiente pós-lesão desfavorável, marcado por inflamação, reorganização da matriz extracelular e cicatriz glial. A polilaminina, biomaterial derivado da organização bioativa da laminina, tem sido proposta como suporte molecular permissivo ao crescimento neurítico e à reconexão axonal, com potencial de integrar abordagens de engenharia tecidual e neuroreabilitação. Este artigo revisa fundamentos biológicos relevantes (laminina–integrinas, matriz extracelular e barreiras à regeneração), discute a aplicabilidade translacional em cães e gatos com trauma raquimedular, propõe desfechos clínicos e funcionais prioritários para avaliação e aborda desafios éticos e regulatórios para pesquisa em animais de companhia. Conclui-se que a hipótese terapêutica é biologicamente plausível, porém depende de validação por ensaios pré-clínicos e clínicos controlados, com padronização de cointervenções e métricas objetivas de desfecho.
Palavras-chave: polilaminina; laminina; lesão medular; trauma raquimedular; cães; gatos; biomateriais; neuroregeneração.
1 Introdução
O trauma raquimedular em cães e gatos é um problema frequente em serviços de emergência e neurologia veterinária, sendo comumente decorrente de atropelamentos, quedas, agressões ou acidentes domésticos. Dependendo do nível da lesão e da extensão do dano, os pacientes podem apresentar desde dor espinhal e ataxia até paraplegia ou tetraplegia, frequentemente acompanhadas de disfunções urinárias, fecais e alterações autonômicas. Além do impacto direto no bem-estar do animal, a condição impõe custos e demanda de cuidados prolongados aos tutores.
Do ponto de vista fisiopatológico, a lesão medular traumática envolve um componente mecânico inicial (lesão primária) e uma cascata subsequente (lesão secundária) com inflamação, excitotoxicidade, estresse oxidativo, isquemia, apoptose e desmielinização. Ao longo do tempo, consolidam-se alterações estruturais e moleculares que limitam a regeneração, incluindo formação de cicatriz glial e remodelamento da matriz extracelular, gerando um microambiente inibitório ao rebrotamento axonal. Mesmo quando a estabilização vertebral e a descompressão são bem-sucedidas, a reconexão de vias interrompidas é incomum, e parte importante da recuperação clínica observada é atribuída a plasticidade e compensação funcional.
Nesse contexto, biomateriais e estratégias de engenharia tecidual têm sido investigados com o objetivo de fornecer suporte físico e molecular que favoreça crescimento neurítico, reorganização tecidual e integração funcional. A polilaminina, baseada na organização bioativa de moléculas de laminina, é proposta como arcabouço permissivo para reconexão axonal em lesões do sistema nervoso central. Considerando a relevância clínica do trauma raquimedular em cães e gatos, bem como o valor translacional de casos espontâneos em medicina comparada, torna-se pertinente discutir criticamente fundamentos, potenciais aplicações e requisitos de validação científica para a polilaminina na medicina veterinária.
2 Bases biológicas: matriz extracelular, cicatriz glial e regeneração no SNC
A matriz extracelular (MEC) exerce papel fundamental na organização tecidual, adesão celular e sinalização. No tecido nervoso, a MEC participa de eventos do neurodesenvolvimento e da plasticidade, influenciando migração e diferenciação celular, bem como crescimento axonal. Em lesões do sistema nervoso central, entretanto, o microambiente se torna progressivamente desfavorável à regeneração.
Após trauma medular, a formação de cicatriz glial constitui evento central. A cicatriz envolve ativação de astrócitos e outras células gliais, além de deposição de componentes da MEC, atuando inicialmente como mecanismo de contenção e proteção. No entanto, sua consolidação resulta em barreiras físicas e bioquímicas ao crescimento axonal. Assim, intervenções regenerativas bem-sucedidas tendem a necessitar de estratégias que: (i) reduzam a toxicidade do ambiente inflamatório inicial, (ii) forneçam substratos permissivos ao crescimento neurítico, (iii) orientem a reorganização tecidual e (iv) favoreçam integração sináptica funcional.
3 Laminina e interações laminina–integrinas: implicações para crescimento axonal
A laminina é uma glicoproteína de destaque na MEC, associada à adesão celular e ao crescimento axonal. Interações entre laminina e receptores celulares, como integrinas, participam de processos de migração e extensão neurítica. Em termos conceituais, materiais baseados em laminina podem fornecer sinais permissivos para neuritos e favorecer organização do tecido reparativo.
Entretanto, a presença de um substrato permissivo não garante, por si só, restauração funcional. A recuperação clínica exige reconexões adequadas, remielinização compatível e integração dos circuitos ao controle motor e sensitivo. Além disso, a janela temporal (aguda, subaguda ou crônica) modifica as principais barreiras biológicas e, portanto, altera o potencial de resposta a terapias baseadas em MEC.
4 Polilaminina: conceito, hipótese de mecanismo e plausibilidade translacional
A polilaminina pode ser compreendida como uma organização bioativa de laminina com potencial de atuar como “scaffold” molecular. A hipótese central é que a organização estrutural fornecida por esse biomaterial promova microambiente mais favorável ao crescimento neurítico e à reconexão axonal, funcionando como suporte para reorganização pós-lesão.
No contexto translacional, cães com lesão medular espontânea são frequentemente citados como modelos relevantes, pois apresentam heterogeneidade real de lesões, comorbidades e padrões de recuperação semelhantes aos observados na clínica humana. Para a medicina veterinária, isso representa oportunidade e desafio: oportunidade por permitir avaliação de desfechos clínicos reais; desafio porque a variabilidade pode reduzir poder estatístico e dificultar inferência causal, exigindo delineamentos controlados, estratificação por gravidade e padronização de cointervenções (cirurgia, analgesia e reabilitação).
5 Trauma raquimedular em cães e gatos: cenário clínico e limitações terapêuticas
Em cães e gatos, o trauma raquimedular costuma envolver fratura, luxação e/ou contusão medular, frequentemente exigindo estabilização vertebral, suporte intensivo e reabilitação prolongada. O prognóstico depende da extensão do dano medular, da presença de compressão persistente e de achados do exame neurológico, com ênfase na preservação de vias sensitivas profundas quando aplicável. A despeito disso, a variabilidade individual é considerável.
As terapias convencionais incluem estabilização cirúrgica, analgesia multimodal, manejo urinário, prevenção de complicações secundárias e fisioterapia intensiva. Contudo, a regeneração axonal efetiva no SNC é limitada, e muitos pacientes mantêm déficits permanentes. Assim, estratégias adjuvantes devem demonstrar benefício incremental em relação ao padrão de cuidado, sem introduzir riscos desproporcionais.
6 Proposta de aplicação e desenho de avaliação em medicina veterinária (visão metodológica)
Para avaliação científica da polilaminina em cães e gatos com trauma raquimedular, recomenda-se estruturar estudos com:
6.1 População e estratificação
Estratificação por:
- espécie (cão/gato);
- nível lesional (cervical vs toracolombar);
- gravidade neurológica inicial;
- tempo até intervenção;
- padrão de lesão (predominantemente compressiva vs contusiva).
6.2 Cointervenções padronizadas
É crucial padronizar:
- técnica cirúrgica/estabilização conforme protocolo;
- analgesia e suporte pós-operatório;
- reabilitação (frequência, tipo e adesão).
6.3 Desfechos prioritários (clínicos e funcionais)
Desfechos devem ser clinicamente significativos e mensuráveis:
- retorno à deambulação funcional (tempo e proporção);
- melhora em escala neurológica padronizada;
- continência urinária;
- dor;
- complicações secundárias;
- qualidade de vida do animal e do tutor (questionários).
6.4 Cegamento e redução de vieses
Quando possível, avaliação por examinador cegado, uso de vídeos de marcha e instrumentos padronizados. Em cenários em que randomização seja inviável, delineamentos com pareamento e ajuste multivariado devem ser considerados, com reconhecimento explícito de limitações.
7 Aspectos éticos e regulatórios
O uso de biomateriais em animais de companhia requer aprovação por comitê de ética em uso animal (CEUA), consentimento informado do tutor e plano de monitoramento de segurança. A comunicação deve ser transparente quanto ao caráter experimental e à ausência de garantia de benefício. Devem ser definidos critérios de resgate terapêutico e interrupção individual, preservando bem-estar como prioridade.
8 Discussão
A polilaminina apresenta plausibilidade biológica ao se apoiar em mecanismos de MEC e laminina relacionados a adesão e crescimento neurítico. Todavia, a tradução clínica depende de demonstrar não apenas alterações histológicas ou de conectividade, mas ganhos funcionais sustentados e clinicamente relevantes. Em neurologia veterinária, a interpretação de melhora exige cautela, pois reabilitação intensiva, plasticidade e recuperação espontânea podem produzir avanços significativos e confundir a atribuição causal.
Para reduzir esse risco, estudos devem incorporar comparadores apropriados e reabilitação padronizada, além de desfechos objetivos e acompanhamento longitudinal. Também é necessário delimitar a janela terapêutica e o fenótipo lesional em que a intervenção teria maior plausibilidade (agudo/subagudo vs crônico; compressivo vs contusivo). Adicionalmente, questões de custo, acesso e logística influenciam viabilidade e generalização dos achados.
9 Conclusão
A polilaminina constitui uma estratégia promissora no campo de biomateriais aplicados à neuroregeneração e pode representar uma linha de investigação relevante para trauma raquimedular em cães e gatos. Entretanto, sua incorporação à prática clínica veterinária deve ser precedida por estudos pré-clínicos e ensaios clínicos controlados que estabeleçam segurança, dose/forma de aplicação e benefício funcional incremental em relação ao cuidado padrão, dentro de marcos éticos e regulatórios robustos.
Referências (ABNT)
DEWEY, Curtis W.; DA COSTA, Ronaldo C. Veterinary Neuroanatomy and Clinical Neurology. 3. ed. Hoboken: Wiley-Blackwell, 2015.
ROSSIGNOL, Serge; FRIGON, Alain. Recovery of locomotion after spinal cord injury: Some facts and mechanisms. Annual Review of Neuroscience, v. 34, p. 413-440, 2011.
YAMADA, Kenneth M.; SEKIGUCHI, Kaori. Molecular basis of laminin-integrin interactions. Current Opinion in Cell Biology, v. 36, p. 35-41, 2015.
SAMPAIO, Tatiana Coelho de. Estudos experimentais sobre polilaminina e regeneração medular. Rio de Janeiro: Universidade Federal do Rio de Janeiro, relatórios técnicos, [s.d.].
Polylaminin in Veterinary Medicine: Translational Perspectives for Treating Traumatic Spinal Cord Injury in Dogs and Cats
Abstract
Traumatic spinal cord injury (SCI) in dogs and cats is a frequent cause of paralysis, pain, and reduced quality of life, commonly associated with vertebral fractures, luxations, and spinal cord contusion. Even with modern surgical stabilization, multimodal analgesia, intensive nursing, and rehabilitation, full functional recovery remains uncommon in severe cases. This limitation reflects the intrinsically low regenerative capacity of the central nervous system (CNS) and the development of a hostile post-injury microenvironment characterized by inflammation, extracellular matrix (ECM) remodeling, and glial scar formation. Polylaminin, a biomaterial derived from the bioactive organization of laminin molecules, has been proposed as a permissive molecular scaffold that may support neurite outgrowth and axonal reconnection, aligning with contemporary tissue engineering and regenerative medicine strategies. This review summarizes the biological rationale linking laminin–integrin signaling to axonal growth, discusses translational opportunities and pitfalls of moving a CNS biomaterial concept into companion animal neurology, outlines priority clinical and functional outcomes for veterinary trials, and highlights ethical and regulatory requirements for responsible research in client-owned animals. While the therapeutic hypothesis is biologically plausible, veterinary use must be preceded by controlled safety assessments and well-designed clinical studies with standardized co-interventions and objective outcome measures.
Keywords: polylaminin; laminin; traumatic spinal cord injury; dog; cat; biomaterials; neuroregeneration; veterinary neurology.
1. Introduction
Traumatic spinal cord injury (SCI) in small animal practice represents a major neurological emergency and a substantial welfare challenge. In dogs and cats, SCI most often occurs secondary to high-energy trauma such as road traffic accidents, falls, crush injuries, and bite-related events, frequently leading to vertebral fractures, luxations, instability, and spinal cord contusion. Clinical presentations range from spinal pain and ataxia to paraplegia or tetraplegia, sometimes accompanied by autonomic dysfunction (urinary retention/incontinence, fecal dysfunction) and secondary complications (pressure sores, urinary tract infections, respiratory compromise in cervical injuries).
Standard-of-care management typically includes stabilization of systemic status, pain control, diagnostic imaging, surgical stabilization and/or decompression when indicated, intensive nursing, bladder management, and structured rehabilitation. However, many patients—particularly those with severe neurological deficits—fail to regain normal locomotion or continence. This reflects, in part, the limited intrinsic regenerative capacity of the mammalian central nervous system (CNS), combined with complex secondary injury cascades and long-term inhibitory changes at the lesion site.
Within this framework, regenerative strategies—including cellular therapies, neuromodulation, and biomaterials—have gained attention. Biomaterials are particularly attractive because they may provide a physical and molecular scaffold to support tissue organization, guide axonal growth, and modulate the lesion microenvironment. Polylaminin, a Brazilian-developed biomaterial derived from the bioactive organization of laminin, has been discussed in translational contexts for CNS repair. Given the clinical burden of SCI in companion animals and the potential role of dogs as translational models due to naturally occurring disease, evaluating polylaminin from a veterinary perspective is timely. Still, any movement from plausibility to clinical adoption must be guided by evidence, safety, and ethical rigor.
2. Traumatic Spinal Cord Injury in Dogs and Cats: Clinical Context
2.1 Common mechanisms and lesion patterns
Traumatic SCI in dogs and cats typically combines:
- Mechanical instability (fracture/luxation)
- Compression (bone fragments, disc material, hemorrhage, swelling)
- Contusion and hemorrhage within the cord
- Secondary ischemia and edema
The lesion phenotype may differ between species and even between trauma scenarios. Cats often present after high-rise falls and motor vehicle trauma, while dogs commonly experience road traffic accidents and blunt trauma. Mixed injuries are common, and management frequently requires both orthopedic/neurosurgical decision-making and intensive supportive care.
2.2 Prognostic considerations
Prognosis in veterinary SCI is multifactorial and depends on:
- neurological severity at presentation
- lesion location (cervical vs thoracolumbar)
- time to definitive stabilization/decompression (when appropriate)
- imaging findings (compression, hemorrhage, cord swelling)
- development of complications (e.g., infections, pressure sores)
In clinical practice, serial neurological examinations and standardized grading systems help guide prognosis and monitor improvement. However, heterogeneity in trauma type and the complexity of supportive care can confound outcome interpretation, reinforcing the need for controlled study designs when evaluating novel adjunct therapies.
3. Pathophysiology: Why CNS Repair Is So Limited
3.1 Primary and secondary injury
The initial mechanical insult (primary injury) disrupts axons, blood vessels, and neural tissue. Secondary injury mechanisms then expand damage through:
- excitotoxicity and ionic imbalance
- oxidative stress
- neuroinflammation and immune cell infiltration
- edema and microvascular dysfunction
- demyelination and apoptotic pathways
These cascades evolve over time, which matters when considering intervention windows. Therapies aimed at acute neuroprotection may differ from those targeting subacute or chronic regeneration.
3.2 Extracellular matrix remodeling and the glial scar
After injury, the lesion site undergoes major ECM remodeling and glial responses. A glial scar forms—initially protective by containing damage and limiting spread, but later inhibitory to axonal regeneration. The scar environment can hinder regrowth through physical barriers and molecular signals that reduce axonal extension and synaptic integration.
Thus, successful functional repair likely requires a combination of:
- limiting secondary injury
- creating a permissive growth environment
- providing guidance for axons and neurites
- enabling meaningful circuit reconnection and remyelination
4. Laminin Biology and Laminin–Integrin Signaling
Laminins are key ECM glycoproteins involved in cell adhesion, differentiation, migration, and neurite outgrowth. Laminin interacts with cell-surface receptors (including integrins) that translate ECM cues into intracellular signaling cascades that can influence cytoskeletal organization and growth cone dynamics.
From a regenerative medicine standpoint, laminin-based scaffolds are attractive because they can mimic supportive developmental cues. Nonetheless, laminin signaling does not operate in isolation; it must be interpreted within the broader post-injury microenvironment. Therefore, any laminin-derived or laminin-organized biomaterial must ultimately demonstrate that it supports functional recovery—not merely neurite growth in vitro or structural changes in experimental settings.
5. Polylaminin: Concept and Translational Rationale
Polylaminin can be described as a bioactive organization of laminin molecules that may function as a molecular scaffold. Conceptually, such a scaffold could:
- provide a permissive substrate for neurite extension
- support tissue organization at the lesion interface
- facilitate axonal bridging across disrupted regions
- potentially modulate aspects of ECM-related inhibitory signaling
5.1 Translational relevance in companion animals
Companion animal SCI is clinically relevant and, in dogs, naturally occurring spinal injuries are often viewed as translationally informative. However, translational relevance does not remove the need for rigorous veterinary evidence. A therapy proposed for human SCI cannot be assumed effective or safe in dogs and cats without veterinary-specific testing. Differences in lesion patterns, body size, surgical approaches, and rehabilitation logistics can materially affect outcomes.
5.2 Key questions before veterinary adoption
To responsibly translate polylaminin into veterinary practice, studies must clarify:
- local and systemic safety in dogs and cats (acute and subacute)
- optimal timing (acute/subacute vs chronic)
- delivery method (intraoperative placement, local injection, other)
- compatibility with surgical stabilization materials and infection control
- incremental benefit over standard-of-care plus rehabilitation
- reproducibility across different trauma phenotypes and severities
6. Suggested Clinical Trial Framework for Veterinary Evaluation
A publishable and clinically meaningful veterinary evidence pathway typically includes:
- Controlled preclinical safety evaluation (species-appropriate, dose-ranging when feasible)
- Pilot clinical feasibility study in client-owned animals (focus: safety, recruitment feasibility, adherence to follow-up)
- Prospective controlled clinical trial with standardized co-interventions and robust outcomes
6.1 Study population and stratification
Because traumatic SCI is heterogeneous, stratification is essential. Suggested stratification variables include:
- species (dog vs cat)
- lesion location (cervical vs thoracolumbar)
- neurological severity at baseline
- time from injury to intervention
- instability vs predominantly contusive lesions
- presence of concurrent traumatic injuries
6.2 Standardization of co-interventions
To avoid falsely attributing improvement to the biomaterial, trials should standardize:
- surgical stabilization protocols (as much as possible)
- analgesia and perioperative care
- bladder management
- rehabilitation frequency and content
- home-care guidance and compliance monitoring
6.3 Priority outcomes (clinically meaningful endpoints)
Outcomes should be objective, clinically relevant, and longitudinal:
- time to functional ambulation (clear operational definition)
- neurological scoring changes over time using a standardized scale
- continence outcomes (time to voluntary urination/continence, when applicable)
- pain outcomes using validated behavioral/clinical scales
- complication rates (UTIs, pressure sores, reoperation)
- quality-of-life measures (owner-reported instruments when available)
6.4 Minimizing bias
Recommended strategies include:
- assessor blinding (when feasible)
- video-based gait assessments reviewed by a blinded evaluator
- predefined follow-up schedule (e.g., 7, 14, 30, 60, 90, 180 days)
- intention-to-treat principles and transparent reporting of losses to follow-up
7. Ethical and Regulatory Considerations
When studying novel biomaterials in client-owned dogs and cats, ethical requirements typically include:
- approval by an institutional animal ethics committee (e.g., CEUA in Brazil)
- informed owner consent with clear communication of experimental status
- robust analgesia and welfare monitoring
- predefined rescue criteria and stopping rules for adverse events
- data protection and transparency in reporting results (positive or negative)
Given the vulnerability of owners facing distressing neurological injuries, communication must avoid overpromising benefits. Ethical acceptability hinges on plausible benefit, minimized risk, and a scientifically sound protocol capable of generating meaningful knowledge.
8. Discussion
Polylaminin fits within a broader class of ECM-informed biomaterial strategies aimed at improving the permissiveness of the post-injury environment. The biological rationale—leveraging laminin-related signaling and scaffold effects—is coherent with established principles of neurite growth and tissue engineering. However, the gap between neurite outgrowth and functional recovery remains the central challenge in SCI therapeutics. In veterinary medicine, this challenge is compounded by heterogeneity of trauma, variability in rehabilitation adherence, and differences in clinical infrastructure across settings.
Therefore, the most defensible path forward is a staged evidence program emphasizing safety, feasibility, and controlled comparative trials with standardized rehabilitation. Claims of clinical effectiveness should be reserved until supported by appropriately designed veterinary studies. A careful translational approach may ultimately benefit both veterinary patients and the comparative neurology field.
9. Conclusion
Polylaminin is a biologically plausible biomaterial candidate for adjunctive treatment of traumatic spinal cord injury in dogs and cats, potentially supporting a more permissive microenvironment for neurite growth and axonal reconnection. Nonetheless, veterinary implementation should not proceed without controlled safety assessment and rigorous clinical trial validation demonstrating clinically meaningful functional outcomes beyond standard-of-care and rehabilitation. Ethical and regulatory safeguards are essential, particularly in research involving client-owned companion animals.
References (ABNT format)
DEWEY, C. W.; DA COSTA, R. C. Veterinary Neuroanatomy and Clinical Neurology. 3. ed. Hoboken: Wiley-Blackwell, 2015.
ROSSIGNOL, S.; FRIGON, A. Recovery of locomotion after spinal cord injury: Some facts and mechanisms. Annual Review of Neuroscience, v. 34, p. 413-440, 2011.
YAMADA, K. M.; SEKIGUCHI, K. Molecular basis of laminin-integrin interactions. Current Opinion in Cell Biology, v. 36, p. 35-41, 2015.
SAMPAIO, T. C. Estudos experimentais sobre polilaminina e regeneração medular. Rio de Janeiro: Universidade Federal do Rio de Janeiro, relatórios técnicos. [s.d.].
-
Polylaminin in Veterinary Medicine: Translational Perspectives for Treating Traumatic Spinal Cord Injury in Dogs and Cats
Cláudio Amichetti Júnior¹,²
Gabriel Amichetti³¹ Integrative Veterinary Physician – CRMV-SP 75.404 VT; MAPA 00129461/2025; CREA 060149829-SP (Agronomist Engineer). Specialist in Feline and Canine Nutrition, Cannabinoid Medicine, and Natural Feeding, Petclube. Over 40 years of practical experience dedicated to felines and bull-type dogs, focusing on dietary transition and development of well-being protocols.
² Petclube Institutional Affiliation, São Paulo, Brazil.
³ Veterinarian – CRMV-SP 45.592 VT. Specialization in Orthopedics and Small Animal Surgery – Clínica 3RD, Vila Zelina, São Paulo, Brazil.Conflict of interest: The authors declare no conflict of interest.
Journal: Petclube – Science, Genetics and Animal Well-Being.Abstract
Traumatic spinal cord injury (SCI) in dogs and cats is a frequent cause of paralysis, pain, and reduced quality of life, commonly associated with vertebral fractures, luxations, and spinal cord contusion. Even with modern surgical stabilization, multimodal analgesia, intensive nursing, and rehabilitation, full functional recovery remains uncommon in severe cases. This limitation reflects the intrinsically low regenerative capacity of the central nervous system (CNS) and the development of a hostile post-injury microenvironment characterized by inflammation, extracellular matrix (ECM) remodeling, and glial scar formation. Polylaminin, a biomaterial derived from the bioactive organization of laminin molecules, has been proposed as a permissive molecular scaffold that may support neurite outgrowth and axonal reconnection, aligning with contemporary tissue engineering and regenerative medicine strategies. This review summarizes the biological rationale linking laminin–integrin signaling to axonal growth, discusses translational opportunities and pitfalls of moving a CNS biomaterial concept into companion animal neurology, outlines priority clinical and functional outcomes for veterinary trials, and highlights ethical and regulatory requirements for responsible research in client-owned animals. While the therapeutic hypothesis is biologically plausible, veterinary use must be preceded by controlled safety assessments and well-designed clinical studies with standardized co-interventions and objective outcome measures.
Keywords: polylaminin; laminin; traumatic spinal cord injury; dog; cat; biomaterials; neuroregeneration; veterinary neurology.
1. Introduction
Traumatic spinal cord injury (SCI) in small animal practice represents a major neurological emergency and a substantial welfare challenge. In dogs and cats, SCI most often occurs secondary to high-energy trauma such as road traffic accidents, falls, crush injuries, and bite-related events, frequently leading to vertebral fractures, luxations, instability, and spinal cord contusion. Clinical presentations range from spinal pain and ataxia to paraplegia or tetraplegia, sometimes accompanied by autonomic dysfunction (urinary retention/incontinence, fecal dysfunction) and secondary complications (pressure sores, urinary tract infections, respiratory compromise in cervical injuries).
Standard-of-care management typically includes stabilization of systemic status, pain control, diagnostic imaging, surgical stabilization and/or decompression when indicated, intensive nursing, bladder management, and structured rehabilitation. However, many patients—particularly those with severe neurological deficits—fail to regain normal locomotion or continence. This reflects, in part, the limited intrinsic regenerative capacity of the mammalian central nervous system (CNS), combined with complex secondary injury cascades and long-term inhibitory changes at the lesion site.
Within this framework, regenerative strategies—including cellular therapies, neuromodulation, and biomaterials—have gained attention. Biomaterials are particularly attractive because they may provide a physical and molecular scaffold to support tissue organization, guide axonal growth, and modulate the lesion microenvironment. Polylaminin, a Brazilian-developed biomaterial derived from the bioactive organization of laminin, has been discussed in translational contexts for CNS repair. Given the clinical burden of SCI in companion animals and the potential role of dogs as translational models due to naturally occurring disease, evaluating polylaminin from a veterinary perspective is timely. Still, any movement from plausibility to clinical adoption must be guided by evidence, safety, and ethical rigor.
2. Traumatic Spinal Cord Injury in Dogs and Cats: Clinical Context
2.1 Common mechanisms and lesion patterns
Traumatic SCI in dogs and cats typically combines:
- Mechanical instability (fracture/luxation)
- Compression (bone fragments, disc material, hemorrhage, swelling)
- Contusion and hemorrhage within the cord
- Secondary ischemia and edema
The lesion phenotype may differ between species and even between trauma scenarios. Cats often present after high-rise falls and motor vehicle trauma, while dogs commonly experience road traffic accidents and blunt trauma. Mixed injuries are common, and management frequently requires both orthopedic/neurosurgical decision-making and intensive supportive care.
2.2 Prognostic considerations
Prognosis in veterinary SCI is multifactorial and depends on:
- neurological severity at presentation
- lesion location (cervical vs thoracolumbar)
- time to definitive stabilization/decompression (when appropriate)
- imaging findings (compression, hemorrhage, cord swelling)
- development of complications (e.g., infections, pressure sores)
In clinical practice, serial neurological examinations and standardized grading systems help guide prognosis and monitor improvement. However, heterogeneity in trauma type and the complexity of supportive care can confound outcome interpretation, reinforcing the need for controlled study designs when evaluating novel adjunct therapies.
3. Pathophysiology: Why CNS Repair Is So Limited
3.1 Primary and secondary injury
The initial mechanical insult (primary injury) disrupts axons, blood vessels, and neural tissue. Secondary injury mechanisms then expand damage through:
- excitotoxicity and ionic imbalance
- oxidative stress
- neuroinflammation and immune cell infiltration
- edema and microvascular dysfunction
- demyelination and apoptotic pathways
These cascades evolve over time, which matters when considering intervention windows. Therapies aimed at acute neuroprotection may differ from those targeting subacute or chronic regeneration.
3.2 Extracellular matrix remodeling and the glial scar
After injury, the lesion site undergoes major ECM remodeling and glial responses. A glial scar forms—initially protective by containing damage and limiting spread, but later inhibitory to axonal regeneration. The scar environment can hinder regrowth through physical barriers and molecular signals that reduce axonal extension and synaptic integration.
Thus, successful functional repair likely requires a combination of:
- limiting secondary injury
- creating a permissive growth environment
- providing guidance for axons and neurites
- enabling meaningful circuit reconnection and remyelination
4. Laminin Biology and Laminin–Integrin Signaling
Laminins are key ECM glycoproteins involved in cell adhesion, differentiation, migration, and neurite outgrowth. Laminin interacts with cell-surface receptors (including integrins) that translate ECM cues into intracellular signaling cascades that can influence cytoskeletal organization and growth cone dynamics.
From a regenerative medicine standpoint, laminin-based scaffolds are attractive because they can mimic supportive developmental cues. Nonetheless, laminin signaling does not operate in isolation; it must be interpreted within the broader post-injury microenvironment. Therefore, any laminin-derived or laminin-organized biomaterial must ultimately demonstrate that it supports functional recovery—not merely neurite growth in vitro or structural changes in experimental settings.
5. Polylaminin: Concept and Translational Rationale
Polylaminin can be described as a bioactive organization of laminin molecules that may function as a molecular scaffold. Conceptually, such a scaffold could:
- provide a permissive substrate for neurite extension
- support tissue organization at the lesion interface
- facilitate axonal bridging across disrupted regions
- potentially modulate aspects of ECM-related inhibitory signaling
5.1 Translational relevance in companion animals
Companion animal SCI is clinically relevant and, in dogs, naturally occurring spinal injuries are often viewed as translationally informative. However, translational relevance does not remove the need for rigorous veterinary evidence. A therapy proposed for human SCI cannot be assumed effective or safe in dogs and cats without veterinary-specific testing. Differences in lesion patterns, body size, surgical approaches, and rehabilitation logistics can materially affect outcomes.
5.2 Key questions before veterinary adoption
To responsibly translate polylaminin into veterinary practice, studies must clarify:
- local and systemic safety in dogs and cats (acute and subacute)
- optimal timing (acute/subacute vs chronic)
- delivery method (intraoperative placement, local injection, other)
- compatibility with surgical stabilization materials and infection control
- incremental benefit over standard-of-care plus rehabilitation
- reproducibility across different trauma phenotypes and severities
6. Suggested Clinical Trial Framework for Veterinary Evaluation
A publishable and clinically meaningful veterinary evidence pathway typically includes:
- Controlled preclinical safety evaluation (species-appropriate, dose-ranging when feasible)
- Pilot clinical feasibility study in client-owned animals (focus: safety, recruitment feasibility, adherence to follow-up)
- Prospective controlled clinical trial with standardized co-interventions and robust outcomes
6.1 Study population and stratification
Because traumatic SCI is heterogeneous, stratification is essential. Suggested stratification variables include:
- species (dog vs cat)
- lesion location (cervical vs thoracolumbar)
- neurological severity at baseline
- time from injury to intervention
- instability vs predominantly contusive lesions
- presence of concurrent traumatic injuries
6.2 Standardization of co-interventions
To avoid falsely attributing improvement to the biomaterial, trials should standardize:
- surgical stabilization protocols (as much as possible)
- analgesia and perioperative care
- bladder management
- rehabilitation frequency and content
- home-care guidance and compliance monitoring
6.3 Priority outcomes (clinically meaningful endpoints)
Outcomes should be objective, clinically relevant, and longitudinal:
- time to functional ambulation (clear operational definition)
- neurological scoring changes over time using a standardized scale
- continence outcomes (time to voluntary urination/continence, when applicable)
- pain outcomes using validated behavioral/clinical scales
- complication rates (UTIs, pressure sores, reoperation)
- quality-of-life measures (owner-reported instruments when available)
6.4 Minimizing bias
Recommended strategies include:
- assessor blinding (when feasible)
- video-based gait assessments reviewed by a blinded evaluator
- predefined follow-up schedule (e.g., 7, 14, 30, 60, 90, 180 days)
- intention-to-treat principles and transparent reporting of losses to follow-up
7. Ethical and Regulatory Considerations
When studying novel biomaterials in client-owned dogs and cats, ethical requirements typically include:
- approval by an institutional animal ethics committee (e.g., CEUA in Brazil)
- informed owner consent with clear communication of experimental status
- robust analgesia and welfare monitoring
- predefined rescue criteria and stopping rules for adverse events
- data protection and transparency in reporting results (positive or negative)
Given the vulnerability of owners facing distressing neurological injuries, communication must avoid overpromising benefits. Ethical acceptability hinges on plausible benefit, minimized risk, and a scientifically sound protocol capable of generating meaningful knowledge.
8. Discussion
Polylaminin fits within a broader class of ECM-informed biomaterial strategies aimed at improving the permissiveness of the post-injury environment. The biological rationale—leveraging laminin-related signaling and scaffold effects—is coherent with established principles of neurite growth and tissue engineering. However, the gap between neurite outgrowth and functional recovery remains the central challenge in SCI therapeutics. In veterinary medicine, this challenge is compounded by heterogeneity of trauma, variability in rehabilitation adherence, and differences in clinical infrastructure across settings.
Therefore, the most defensible path forward is a staged evidence program emphasizing safety, feasibility, and controlled comparative trials with standardized rehabilitation. Claims of clinical effectiveness should be reserved until supported by appropriately designed veterinary studies. A careful translational approach may ultimately benefit both veterinary patients and the comparative neurology field.
9. Conclusion
Polylaminin is a biologically plausible biomaterial candidate for adjunctive treatment of traumatic spinal cord injury in dogs and cats, potentially supporting a more permissive microenvironment for neurite growth and axonal reconnection. Nonetheless, veterinary implementation should not proceed without controlled safety assessment and rigorous clinical trial validation demonstrating clinically meaningful functional outcomes beyond standard-of-care and rehabilitation. Ethical and regulatory safeguards are essential, particularly in research involving client-owned companion animals.
References (ABNT format)
DEWEY, C. W.; DA COSTA, R. C. Veterinary Neuroanatomy and Clinical Neurology. 3. ed. Hoboken: Wiley-Blackwell, 2015.
ROSSIGNOL, S.; FRIGON, A. Recovery of locomotion after spinal cord injury: Some facts and mechanisms. Annual Review of Neuroscience, v. 34, p. 413-440, 2011.
YAMADA, K. M.; SEKIGUCHI, K. Molecular basis of laminin-integrin interactions. Current Opinion in Cell Biology, v. 36, p. 35-41, 2015.
SAMPAIO, T. C. Estudos experimentais sobre polilaminina e regeneração medular. Rio de Janeiro: Universidade Federal do Rio de Janeiro, relatórios técnicos. [s.d.].

GLUTAMINA NA REDUÇÃO DA PERMEABILIDADE INTESTINAL E DA INFLAMAÇÃO EM CÃES E GATOS: BASES FISIOLÓGICAS, EVIDÊNCIAS EXPERIMENTAIS E IMPLICAÇÕES CLÍNICAS
Trabalho científico apresentado como artigo de revisão na área de Medicina Veterinária, com ênfase em nutrição e gastroenterologia de pequenos animais.
Autores:
Cláudio Amichetti Júnior¹,²
Gabriel Amichetti³
¹ Médico-veterinário Integrativo – CRMV-SP 75.404 VT; MAPA 00129461/2025, CREA 060149829-SP Engenheiro Agrônomo Sustentável, Especialista em Nutrição Felina e Alimentação Natural, Petclube. Com mais de 40 anos de experiência prática dedicados aos felinos, com foco em transição dietética e desenvolvimento de protocolos de bem-estar.
² [Afiliação Institucional Petclube, São Paulo, Brasil]
³ Médico-veterinário CRMV-SP 45.592 VT, Especialização em Ortopedia e Cirurgia de Pequenos Animais – [clínica 3RD Vila Zelina SP]
Autor Correspondente: Cláudio Amichetti Júnior, [dr.claudio.amichetti@gmail.com]
Conflito de Interesses: Os autores declaram não haver conflito de interesses.
Petclube – Ciência, Genética e Bem-Estar Animal
RESUMO
A integridade da barreira intestinal é essencial para a homeostase imunológica e metabólica de cães e gatos. A disfunção dessa barreira, caracterizada pelo aumento da permeabilidade intestinal, está associada a enteropatias crônicas, disbiose e inflamação sistêmica de baixo grau. A glutamina é um aminoácido condicionalmente essencial e constitui o principal substrato energético dos enterócitos e das células do sistema imune intestinal. Evidências experimentais indicam que a glutamina contribui para a manutenção das junções epiteliais, redução da translocação bacteriana e modulação da resposta inflamatória intestinal (Amichetti, 2021). Embora estudos clínicos específicos em cães e gatos ainda sejam limitados, os mecanismos fisiológicos envolvidos são altamente conservados entre mamíferos. Este artigo revisa as bases fisiopatológicas do intestino permeável, os mecanismos de ação da glutamina e as evidências científicas disponíveis, discutindo suas implicações clínicas na medicina veterinária integrativa.
Palavras-chave: glutamina. permeabilidade intestinal. inflamação intestinal. cães. gatos.
1 INTRODUÇÃO
2 GLUTAMINA E A INTEGRIDADE DA BARREIRA INTESTINAL
A glutamina exerce papel fundamental na manutenção da estrutura e função da mucosa intestinal. A deficiência desse aminoácido está associada à atrofia das vilosidades, redução da espessura epitelial e comprometimento das tight junctions, resultando em aumento da permeabilidade intestinal (KIM; KIM, 2017).
Achamrah et al. (2017) demonstraram que a glutamina regula positivamente a expressão de proteínas como claudinas e ocludinas, essenciais para a coesão intercelular. Além disso, atua como precursora da glutationa, importante antioxidante intracelular, protegendo o epitélio intestinal contra o estresse oxidativo induzido por processos inflamatórios.
Modelos experimentais evidenciam que a suplementação com glutamina reduz a translocação bacteriana para linfonodos mesentéricos e órgãos extraintestinais, indicando melhora funcional da barreira intestinal (ZIEGLER et al., 2000).
3 GLUTAMINA E MODULAÇÃO DA INFLAMAÇÃO INTESTINAL
A inflamação intestinal crônica caracteriza-se pela ativação persistente de vias inflamatórias, como o fator nuclear kappa B (NF-κB), e pela produção excessiva de citocinas pró-inflamatórias, incluindo TNF-α e interleucinas.
Estudos experimentais demonstram que a glutamina reduz a ativação do NF-κB e a expressão de citocinas inflamatórias, promovendo um ambiente intestinal favorável à regeneração tecidual (KIM; KIM, 2017). Em modelos de colite, a suplementação com glutamina resultou em menor dano histológico e melhora da função intestinal.Embora a suplementação com L-glutamina seja uma estratégia comum em contextos clínicos específicos, é fundamental reconhecer que a glutamina é naturalmente encontrada em diversos alimentos, desempenhando um papel crucial na ingestão diária de cães e gatos. Uma dieta de alta qualidade e nutricionalmente balanceada é a primeira linha de defesa para garantir o aporte adequado desse aminoácido.
5 CONCLUSÃO
A glutamina apresenta respaldo científico consistente como nutriente essencial para a manutenção da integridade da barreira intestinal e para a modulação da inflamação. Em cães e gatos, seu uso como adjuvante nutricional mostra-se promissor no manejo de condições associadas ao aumento da permeabilidade intestinal, especialmente dentro de protocolos de medicina veterinária integrativa baseados em evidências.
REFERÊNCIAS
(NBR 6023:2018 – ordem alfabética)
ACHAMRAH, N. et al. Glutamine and the regulation of intestinal permeability: from bench to bedside. Current Opinion in Clinical Nutrition and Metabolic Care, v. 20, n. 1, p. 86–91, 2017.
KIM, M. H.; KIM, H. The roles of glutamine in the intestine and its implication in intestinal diseases. International Journal of Molecular Sciences, v. 18, n. 5, p. 1051, 2017.
NEU, J.; SHENOY, V. Glutamine: role in gut protection and immune function. Nutrition, v. 23, n. 1, p. 1–7, 2017.
SOUBA, W. W. Glutamine and intestinal function. JPEN Journal of Parenteral and Enteral Nutrition, v. 15, n. 1, p. 13–22, 1991.
ZIEGLER, T. R. et al. Glutamine supplementation improves intestinal barrier function in experimental models. American Journal of Physiology – Gastrointestinal and Liver Physiology, v. 278, p. G928–G937, 2000.
- ZOONOSES TRANSMITIDAS POR ROEDORES: UMA ABORDAGEM INTEGRADA DE SAÚDE ÚNICA ENVOLVENDO VIGILÂNCIA EPIDEMIOLÓGICA, PODER PÚBLICO, CLÍNICAS VETERINÁRIAS E CONTROLE DE PRAGAS URBANAS
- Dieta Felina, Disbiose Intestinal e a Transição para Alimentos de Baixo Carboidrato: Uma Revisão Fisiológica e Análise do Mercado Norte-Americano
- PETCLUBE – PET FRIEND ECOLOGICAMENTE CORRETO Propósitos e Diferenciais Construídos ao Longo de + 30 Anos
- BPC-157 e TB-500 na medicina veterinária integrativa de pequenos animais: evidências pré-clínicas, mecanismos moleculares e aplicações clínicas na cicatrização de tendões e músculos em cães e gatos
- Novas Perspectivas na Abordagem da Osteoartrite Canina: Uma Revisão Crítica sobre Diagnóstico e Estratégias Terapêuticas Multimodais: Pentosan Polissulfato de Sódio
- Potencial Terapêutico das Raízes de Cannabis sativa L.: Revisão Integrativa da Composição Fitoquímica e Perspectivas Biomédicas