Os protozoários são organismos eucariontes, unicelulares, heterotróficos e podem ser de vida livre ou fazer parte de colônias. Eles apresentam diversas fases em seu ciclo biológico, desde trofozoítos, que são as formas ativas e que exercem a ação patogênica, até os oocistos, que são a forma de resistência e a forma sexuada. Por viverem em meio aquoso, ou seja, são encontrados na água ou em algum líquido, o que torna sua sobrevivência no organismo animal facilitada, já que o mesmo é composto em aproximadamente 70% do seu volume de água, tendo sua instalação mais intensa no trato digestório e sangue, podendo, em menor quantidade, se instalar no sistema genital, linfático, coração e pele.
Devido a tantas formas de doenças que podem acometer animais de diversas espécies é que se faz crucial o controle com medicamentos antiparasitários, além de uma observação diária do comportamento dos mesmos para diagnósticos e tratamentos mais específicos. É fundamental conhecer o ciclo biológico destes protozoários para criar programas de combate e controle do parasita.
COCCIDIOSE
As infecções pelas coccídias (Eimeria, Isospora, Cystoisospora, Cryptosporidium) são infecções parasitárias causadas por protozoários microscópicos que podem afetar diferentes espécies animais. Cães e gatos são suscetíveis às espécies Isospora, Sarcocystis e Hammondia, e somente os gatos são suscetíveis a Toxoplasma e Besnoitia. A coccídia mais comum que afeta estes animais é a do gênero Isospora, sendo I. rivolta e I. felis em gatos, nos cães as espécies I. canis, I. burrowsi, I. neorivolta e I. ohioensis. Animais jovens submetidos a sistemas de confinamento ou estresse podem sofrer infecções clínicas por Isospora sp., Cystoisospora sp., Toxoplasma, Besnoitia, Sarcocystis e Hammondia. Coccídias afetam o trato intestinal frequentemente. Exceto Cryptosporidium parvum, todas as espécies são específicas do hospedeiro. As coccídias mais comuns pertencem ao gêneroCystoisospora, as espécies C. rivolta e C. felis em gatos, nos cães as espécies C. canis, C. burrowsi, C. neorivolta e C. ohioensis.
O filhote fica exposto ao organismo a partir de fezes da mãe, podendo ingerir as fezes contendo cistos que se desenvolvem no intestino do animal. Filhotes lactentes podem eliminar oocistos por até cinco semanas, enquanto os filhotes desmamados os eliminam durante duas semanas, devido a imaturidade do sistema imune. Os cães adultos e gatos podem se infectar através da ingestão de solo contendo cistos coccídias. Eles podem até comer fezes ou intestinos de outros animais infectados, como roedores.
Tratamento
O tratamento consiste em duas drogas que têm elevadas taxas de sucesso. Estas drogas incluem sulfadimetoxina (via oral ou parenteral), na dosagem de 55 mg/kg/dia, em dose única ou fracionada durante 21 dias. Trimetoprim / sulfadiazina também pode ser utilizado. O amprólio pode ser empregado como preventivo em fêmeas adultas 10 dias antes do parto, na proporção de 30 ml da solução de amprólio a 9,6% em 3,8 litros de água de beber, porém seu uso não foi aprovado em alguns países, como Estados Unidos e a União Europeia. Ele atua na regulação da absorção de tiamina pela coccídia, enquanto o modo de ação destas drogas não mata a coccídia nos intestinos, ele apenas ajuda na prevenção do parasita de se reproduzir. Portanto, a velocidade a que o animal se recupera da infecção é muito lenta (cerca de 2 semanas, se o tratamento for adequado), tempo esse que depende do reestabelecimento do equilíbrio do sistema imune do organismo que é atingido pelo parasita.
Em gatos afetados, a associação sulfatrimetoprim pode ser usada na dose máxima de 60 mg/kg, por 1 semana. Para tratamento sintomático, pode-se utilizar a sulfadimetoxina (via oral ou parenteral) na dose de 50 mg/kg no primeiro dia de tratamento e 25 mg/kg, diariamente, por 2 ou 3 semanas.
Outros protocolos de tratamento podem ser usados no combate deSarcocystis, Hammondia, Cystoisospora, Toxoplasma e Neospora, como o uso de Clindamicina oral 12,5 a 18,5 mg/kg 2 vezes ao dia por 4 semanas. Também pode ser usada uma associação de Sulfadianzina 30 mg/kg + Pirimetamina 0,25-0,5 mg/kg/dia a cada 12 horas por 3 a 4 semanas.
TOXOPLASMOSE
O Toxoplasma gondii é um coccídio que parasita o intestino delgado de membros da família Felidae, inclusive o gato doméstico. Estes animais constituem os hospedeiros definitivos deste parasito, portanto eliminam seus oocistos nas fezes e contaminam o meio ambiente. Após um período de 1 a 5 dias, os oocistos esporulam, tornando-se infectantes para um grande número de espécies de animais de sangue quente, inclusive o próprio gato, o cão e o homem. Nestes animais, hospedeiros intermediários, os esporozoítos liberados dos oocistos penetram nas células intestinais e se multiplicam. Invadem também linfonodos, onde formam taquizoítos que se espalham por todos os tecidos do hospedeiro, inclusive cérebro, músculos estriados e fígado. Pode também ocorrer migração transplacentária. O cão, apesar de não ser hospedeiro definitivo, contribui na disseminação mecânica desta protozoose, e ogato, que é o hospedeiro definitivo, está relacionados com a produção e eliminação dos oocistos, favorecendo a perpetuação da doença, uma vez que somente nele ocorre a reprodução sexuada dos parasitos.
Cerca de 60% dos animais de estimação que têm toxoplasmose pode se recuperar com o tratamento. A recuperação é menos provável em animais novos ou que possuem a supressão severa do seu sistema imune.
Tratamento
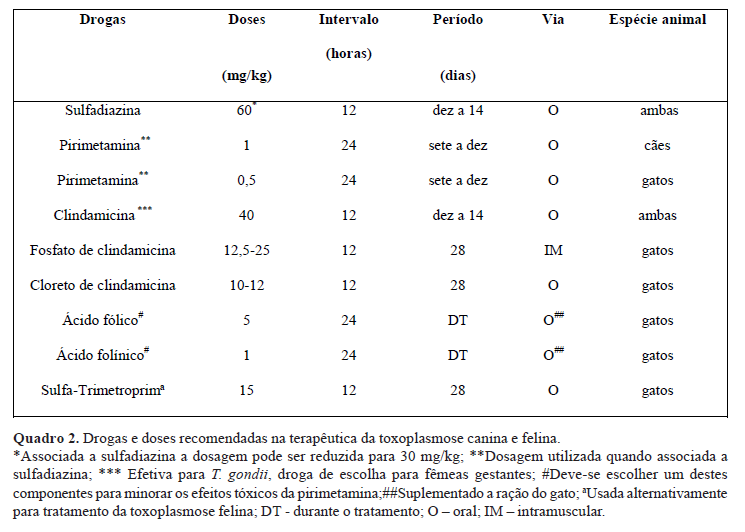
Em uma revisão das alternativas terapêuticas utilizadas para cães foi relatado o uso de sulfadiazina, pirimetamina, clindamicina, fosfato de clindamicina, e cloreto de clindamicina, lembrando-se que estas drogas são utilizadas, em sua maioria, próximo às doses tóxicas para que sejam efetivas, devendo ser utilizado tratamento de apoio, de acordo com os sinais apresentados pelos animais.
Não existe um tratamento completamente satisfatório. A clindamicina é o medicamento de escolha para cães e gatos, que é bem absorvida quando administrada por via oral. Liga-se facilmente às proteínas plasmáticas, distribuindo-se por vários tecidos, inclusive atravessa a barreira placentária, porém não atinge o sistema nervoso central. Para cães com toxoplasmose sistêmica, recomenda-se a dose 10-40 mg/kg via oral, dividida em 3 a 4 vezes/dia; para gatos , recomenda-se 40 mg/kg via oral, divididos em 3 vezes/dia, durante 14 dias. Embora se tenha relatado a utilização de clindamicina, que tem sucesso para o tratamento da miosite provocada pelo agente, a mesma não alcança concentrações terapêuticas, no sistema nervoso central. A toxoplasmose ocular felina deve ser tratada com clindamicina na dose de 12 mg/kg, duas vezes ao dia, durante 4 semanas, ou sulfa-trimetoprim na dose de 15 mg/kg, duas vezes ao dia, durante 4 semanas.
Em gatos, como terapia adjuvante contra uveíte, pode ser administrado colírio de prednisona a 1%. Uma combinação da droga pirimetamina com a sulfadiazina (Tribrissen) foi descrita como eficaz contra taquizoítos, mas não contra bradizoítos, porém é bastante tóxica em gatos.
Sulfonamidas, inibidores do dihidrofosfato redutase e timodilato sintetase e antibióticos ionóforos (lasolocida, narasina e salinomicina), macrolídeos, tetraciclinas e lisonaminas tem ação sobre taquizoítos, e drogas como metronidazol, paramomicina e roxarsona exercem pouca ou nenhuma atividade sobre estas formas evolutivas de multiplicação rápida, sendo a associação de medicamentos mais eficiente. Sinergismo pode ocorrer em sulfonamidas com pirimetamina, monesina ou toltrazuril e sulfonamidas com ormetropina, diaveridina e trimetropin, cloridrato de clindamicina e sulfa associada ao trimetropin.
Cloridrato de clindamicina pode ser utilizado na dosagem de 3 a 20 mg / Kg, e também, na posologia de 12,5 a 25 mg / Kg, por via oral, a cada 12 horas por uma a duas semanas para encurtar o tempo de eliminação do oocisto. Os sinais clínicos da toxoplasmose se resolvem dentro de dois a quatro dias com a administração deste medicamento.
Ácido folínico (0,5 a 5 mg /dia) pode ser empregado para prevenção das complicações hematológicas ocasionadas pelo tratamento com pirimetamina. Fármacos contra Toxoplasma em combinação com corticosteróides tópicos, orais ou parenterais, podem ser utilizados para evitar danos oculares secundários à inflamação. A recorrência é comum se a duração do tratamento for menor que quatro semanas e havendo imunodeficiência, o prognóstico é ruim.
Fonte: SARAIVA et al., 2008.
Medicamentos anticoccidianos:
Pirimetamina: é um fármaco que atua na inibição da enzimadihidrofolato redutase(DHFR), a qual é importante na síntese doácido fólico.
Clindamicina:é um fármaco da classe das lincosaminas que age inibindo a síntese proteica. Atua como um agente bacteriostático, penetra no meio intracelular. A clindamicina possui atividade imunoestimuladora, pois potencializa a opsonização e acelera a quimiotaxia e fagocitose dos leucócitos. É absorvida por via oral e parenteral. Pode ser ingerida concomitantemente com os alimentos, sem prejuízo à sua absorção. Distribui-se amplamente pelos tecidos. Não atravessa satisfatoriamente a barreira hematoencefálica, porém atravessa a barreira placentária. Apresenta elevada concentração no tecido ósseo e articular. Atravessa as membranas celulares atingindo elevadas concentrações no meio intracelular. É metabolizada no fígado e a eliminação dos seus metabólitos é pelaurina,bileefezes.
Amprólio (antagonista de tiamina): atua na regulação da absorção de tiamina pela coccídia, enquanto a sulfaquinoxalina atuam na inibição das vias metabólicas do ácido fólico e do ácido para-aminobenzoico (PABA). A administração de 125 ppm proporciona uma boa eficácia contra um inóculo misto de Eimeria acervulina, E. maxima, E. brunetti, E. tenella. A eficiência do amprólio contra a E. acervulina e a E. tenella é comprovada principalemnte quando associado à sulfaquinoxalina. A associação de 240 ppm de amprólio e 180 ppm de sulfaquinoxalina é eficaz contra E. acervulina, E. maxima, E necatrix, E. brunetti e E. tenella. As associações destas substâncias são recomendadas, pois ocorre o sinergismo dos efeitos destes medicamentos contra as eimerias. Relatos indicando a resistência de alguns isolados de E. acervulina têm sido demonstrados, porém a resistência a este composto ocorre lenta e parcialmente. O amprólio age nos esquizontes de 1ª e 2ª geração.
Sulfonamidas: age contra esquizontes de 2ª geração, sendo menos efetiva contra os estágios assexuados das eimerias. Têm como mecanismo de ação o bloqueio das vias metabólicas do ácido fólico e do PABA. Dentro do grupo destaca-se a sulfaquinoxalina como a mais potente e de menor toxicidade, apesar de apresentar espectro de ação limitado a algumas espécies de eimerias.
Toltrazurila (triazinona simétrica): pertence à classe das triazinonas simétricas, com propriedades coccidicidas de alta eficiência. Atua em diferentes formas evolutivas do parasito, principalmente nos esquizontes, nos macro e microgametócitos, alterando a função da cadeia respiratória e as enzimas mitocondriais.
Trimetoprima: é um análogo doácido fólicoe como tal o substitui naenzimadihidrofolato reductase bacteriana que o sintetiza. É, portanto, umantagonistado ácido fólico, inibindo a sua formação pelabactéria. O ácido fólico é essencial para a replicação das bactérias, já que é usado na duplicação doDNA. Este antibiótico não mata as bactérias, mas inibe a sua multiplicação (é bacteriostática) permitindo aosistema imuneelimina-las facilmente. A trimetoprima é ativa contra a maioria dos patógenos bacterianos comuns. Ela é, às vezes, usada em uma mistura com sulfametoxazol, em uma combinação chamada de co-trimoxazol. Como as sulfonamidas inibem a mesma via metabólica bacteriana, porém acima do local de ação da dihidrofolato redutase, elas podem potencializar a ação da trimetoprima.
REFERÊNCIAS
SPINOSA, H.S; GÓRNIAK, S.L; BERNARDI, M.M. Farmacologia Aplicada à Medicina Veterinária. 5ª ed., Guanabara Koogan, Rio de Janeiro, 2011.
SARAIVA, K. D. B. et al. Toxoplasmose canina: aspectos clínicos e patológicos. Ciências Agrárias, v. 29, n. 1, p. 189-202, 2008.
FONSECA, A. H. Coccidiose em animais domésticos. Universidade Federal Rural do Rio de Janeiro.
GERMANI, C. F.; CAETANO, M. T.; PACHECO, F. A. A. Toxoplasmose animal no Brasil. Acta Scientiae Veterinariae. 37(1): 1-23, 2009.
NEGRI, D.; CIRILO, M. B.; SALVARANI, R. S.; NEVES, M. F. Toxoplasmose em cães e gatos. Revista científica eletrônica de medicina veterinária. Ano VI, n. 11, 2008.
BABESIOSE
A Babesiose é uma doença protozoariana, provocada pela Babesia canis, que parasita as hemácias e as destróis, resultando em anemia hemolítica do tipo regenerativa. Sua transmissão se dá pelo carrapato castanho (Rhipicephalus sanguineos, Dermacentor spp., Haemaphysalis leachi e Hyalomma plumbeum) ou por transfusões sanguíneas. A Babesia canis é um hematozoário relativamente grande que parasita as hemácias, apresentando-se sob formas arredondadas, irregulares e em pêra. Formas arredondadas ou ameboides podem ser encontradas no plasma sanguíneo.
Figura 1 Formas intra-eritrocíticas de Babesia canis. Sangue periférico de cão.
Fonte: Gardiner et al., 1998
Animais de áreas onde há estabilidade enzoótica para essas parasitoses adquirem a infecção sem apresentar sintomatologia clínica aguda. Por outro lado, aqueles de regiões indenes, quando introduzidos numa área onde existe o hematozoário, sofrem a doença de forma severa, que pode levar ao óbito.
O tratamento da babesiose canina está direcionado para o controle do parasita, moderação da resposta imune e tratamento sintomático. Alguns medicamentos usados com essa finalidade foram atualmente substituídos por outros mais eficientes e com maior margem de segurança. O azul tripan, por exemplo, era administrado na dosagem de 10 mg/kg em solução a 1%, via intravenosa, mas tinha um alto risco, já que se ocorresse extravasamento acidental da veia, causaria necrose tecidual.
Os fármacos mais recomendados atualmente são o aceturaro de diminazeno (uma diamidina) e o dipropionato do imidocarb (uma cabanilida), que serão descritos a seguir:
Diminazeno
Diminazeno é a droga comumente usada em todo mundo e é efetiva para o tratamento da B. canis quando administrada pela via intramuscular, em dose única de 2,5 a 3,5 mg/kg. Porém, para o tratamento da B. gibsoni, a dose deve ser repetida após 24 horas.
As diamidinas interferem na glicólise e também na síntese do DNA do parasita, ocasionando dilatação da membrana de organelas, dissolução do citoplasma e destruição da membrana de organelas, dissolução do citoplasma e destruição do núcleo. As diamidinas acumulam-se no fígado e rins, e entram na circulação fetal; além disso, pequenas quantidades ficam acumuladas no sistema nervoso central durante alguns meses.
Esse medicamento é bem tolerado, mas em doses terapêuticas múltiplas em cães podem causar lesões nervosas graves, principalmente ao nível do cerebelo, mesencéfalo e tálamo, além de degeneração gordurosa no fígado, rins, miocárdio e musculatura esquelética.
Dipropinato de imidocarb
O dipropinato de imidocarb também é muito efetivo no tratamento da babesiose, sendo recomendado na dosagem de 5 a 7 mg/kg, por via intramuscular ou subcutânea sendo recomendada duas aplicações com um intervalo de quatorze dias. A fenamidinina também é uma opção, na dose de 15 mg/kg/dia por via subcutânea, em dois dias consecutivos.
Este fármaco atua provocando alterações morfológicas e funcionais do núcleo e do citoplasma do parasita. Este composto apresenta tendência de se depositar no rim e é reabsorvido de forma inalterada, sendo metabolizado pelo fígado.
Cães de áreas onde não há B. canis e que viajem para áreas endêmicas podem ser tratados profilaticamente com uma injeção subcutânea de imidocarb na dose de 6 mg/kg, ficando protegidos por duas semanas, e de doxiciclina* na dose de 10 mg/kg, duas vezes ao dia por onze dias.
*A doxiciclina pertence ao grupo das tetraciclinas e, apesar de ser um antibiótico bacterisotático, por inibir a síntese proteica dos microorganismos sensíveis, também possui ação antimicrobiana sobre alguns protozoários, como a Babesia canis.
Efeitos Colaterais
Os efeitos colaterais que podem ser observados com o tratamento com o cão imidocarb ou diamidinas são: depressão, vocalização contínua, opistótono, ataxia, rigidez extensora, nistagmo e convulsões. Outros efeitos adversos apresentados pelos animais incluem salivação trasitória, diarreia, dispneia, lacrimejamento, depressão e vômitos. Também podem apresentar dor no local de aplicação. Para evitar efeitos colinérgicos indesejados, recomenda-se o uso do sulfato de atropina na dosagem de 0,04 mg/kg, dez minutos antes da aplicação do imidocarb.
CRIPTOSPORIDIOSE
Cryptosporidium é um coccicídio que infecta uma ampla variedade de vertebrados, incluindo o homem. O parasito se localiza principalmente no intestino delgado dos mamíferos e aves. Em cães infectados naturalmente, foram isolados oocistos de C.parvum e C.canis, sendo o C. muris encontrado em cães infectados experimentalmente. Dessas três espécies acredita-se que o C. canis seja a única clinicamente significante para cães.
É considerado um parasito oportunista; em hospedeiros imunocompetentes a infecção é auto-limitante, com duração de poucos dias a três semanas. Em hospedeiros imunocomprometidos a infecção pode resultar em diarreia crônica debilitante, desidratação, má-absorção, enfraquecimento progressivo e morte. No entanto, em indivíduos muito novos ou velhos ou em tratamento que possa causar imunossupressão são os mais severamente afetados. Estes animais frequentemente precisam de tratamento para eliminar o parasito.
Fármacos como a azitromicina, tilosina, paromomicina e nitazoxanida têm sido utilizados em cães com criptosporidiose, mas o número de estudos publicados ainda é reduzido o que não permite obter protocolos seguros e consistentes, devendo o tratamento ser ajustado de acordo com as necessidades de cada paciente. A paromicina não deve ser administrada a animais com diarreia devido a possibilidade de ocorrer absorção com consequente nefrotoxicidade.
Protocolos para o tratamento de infecções por Cryptosporidium no cão.
|
Fármaco |
Protocolo |
|
Azitromicina |
10mg/kg, PO, SID, até resolução dos sinais clínicos. |
|
Nitazoxanida |
25 mg/kg, PO, durante pelo menos 7 dias. |
|
Paromomicina |
125 a 165 mg/kg, PO, SID ou BID durante pelo menos 5 dias. |
|
Tilosina |
10 a 15 mg/kg, PO, BID ou TID, durante 21 dias. |
Fonte: Scorza e Tangtrongsup, 2010
REFERÊNCIAS
MELO, F. L.; LEBRE, C. R. Rastreio de parasitas gastrintestinais e seu impacto zoonótico em cães de canil da cidade de Lisboa. Universidade Técnica de Lisboa. Lisboa. 2011
PIMENTEL, F. F.; ALMEIDA, A. J. de; OLIVEIRA, F. C. R. de; EDERLI, B. B. Efeito do tratamento com nitazoxanida na criptosporidiose canina. Arq. Ciênc. Vet. Zool. UNIPAR, Umuarama, v. 14, n. 2, p. 107-112, jul./dez. 2011.
GARDINER, C.H.; FAYER, R.; DUBEY, J.P. An Atlas of Protozoan Parasites in Animal Tissues. Ed. 2. Armed Forces Institute of Pathology, Washington, 1998
FIGUEIREDO, M.R. Babesiose e erliquiose caninas. Rio de Janeiro, 2007
CORREA, A.R. et al. Babesiose canina: relato de caso. Revista científica eletrônica de medicina veterinária. Ed. 4, 2005
ANTONIO, N.S.; OLIVEIRA, A.C.; ZAPPA, V.; Babesia canis: relato de caso. Revista eletrônica de medicina veterinária. São Paulo. Ed.12, 2009
ANDRADE, E.S.; Infecções causadas por hematozoários em cães e gatos de ocorrência no Brasil: semelhanças e particularidades. Porto Alegre, 2007.
SPINOSA, H.S.; GÓRNIAK, S.L.;BERNARDI, M.M.; Farmacologia Aplicada à Medicina Veterinária. São Paulo: Editora Guanabara Koogan, p. 502-503, 2002.
GIARDÍASE
A giardíase é uma infecção comum em animais, sendo causada por um protozoário flagelado do gênero Giardia, pertencente à ordem Diplomonadida(URQUHART et al., 1987). Os animais eliminam os cistos de parasitas nas fezes após um período de pré-patência de uma a duas semanas, neste período estes podem apresentar ou não sinais clínicos da enfermidade (VIGNARD-ROSEZ; ALVES;BLEICH, 2006). Giardia spp.., em sua forma parasitária, o trofozoíta, se prende às células epiteliais do intestino delgado, causando-lhes lesões. Em animais jovens, sobretudo cães, altas infestações podem causar enterites, com episódios intercalados de parada do trânsito intestinal (constipação) e diarreias.
Dos protozoários que freqüentemente acometem os animais e o homem, Giardia spp. tem despertado grande interesse, pelo seu potencial como agente de zoonose, além de causar, em animais jovens, diarreia intermitente com comprometimento da digestão e absorção de alimentos, acarretando desidratação, perda de peso e morte. Os sinais clínicos podem ser autolimitantes em alguns pacientes e a doença grave ocorre em filhotes e em animais com doenças concomitantes ou debilitados (ROBERTS-HOMSON et al., 1976; ADAM, 1991).
Tratamento:
- Metronidazol
Esse medicamento, após entrar na célula-alvo (trofozoíto), interage com o DNA do protozoário, ocasionando perda de sua estrutura helicoidal e quebra das alças dessa estrutura. Pelo fato de ser pouco solúvel em água e etanol, recomenda-se sua administração por via oral. Parte deste medicamento é biotransformada e aproximadamente 50% são excretados inalterados na urina. É empregado na dose de 25 mg/kg duas vezes ao dia por cinco dias, em cães; e para gatos a dose é de 12-25mg/kg duas vezes ao dia, por 5 dias. Cães tratados com altas doses deste medicamento, tendem a apresentar sinais de intoxicação com consequente disfunção do sistema nervoso central, sendo representados por ataxia, tremores, nistagmo vertical, opistótono, espasmos de musculatura lombar e dos membros posteriores e cauda caída.
- Cloridrato de Quinacrina ou cloridrato de mepacrina
É administrado, geralmente, por via oral ou, com menor frequência, pela via intramuscular. Distribui-se nos tecidos, com tendência de se acumular no fígado, baço, pulmões e glândulas adrenais. Sua eliminação faz-se lentamente pela urina e quantidades muito pequenas são eliminadas pelas secreções corpóreas (bile, saliva, suor, leite).
Recomenda-se para animais de grande porte a dose de 200mg/animal, três vezes no primeiro dia e duas vezes nos cinco dias subsequentes. Para cães de raças pequenas é recomendado a dose de 100 mg, duas vezes no primeiro dia e uma vez ao dia por mais 5 dias. Para filhotes, utilizam-se 50 mg duas vezes ao dia, durante cinco dias. Sugere-se administração de bicarbonato para prevenir vômitos. Para cães com fibrilação auricular, a dose de 2,64 mg/kg, pela via intravenosa, permite reestabelecer o ritmo sinusal normal.
Doses a cima do recomendado podem originar um quadro toxico, representado por vômitos e distúrbios das atividades motora e psicomotora tanto em cães como em gatos.
- Tinidazol
Fármaco da mesma classe que o metronidazol (classe dos nitroimidazois), sendo recomendado na dose de 44 mg ao dia, durante 3 dias.
- Anti-helminticos
Outros fármacos utilizados para o tratamento da giardíase são os anti-helmínticos, sendo os mais utlizados os benzimidazóis. Indica-se albendazol na dose de 25 mg/kg, duas vezes ao dia, durante 2 dias, suspeita-se que tenha efeito teratogênico, não sendo recomendado para fêmeas prenhes. Já fembendazol, é indicado na dose de 50mg/kg/dia, durante 3 dias (não foi testado em gatos).
- Furazolidona
Essa droga sofre uma ativação reduzida no trofozoíto, que é pouco provável ao metronidazol, essa redução provavelmente ocorre via uma NADH oxidase (38, 244). Seu efeito de morte está relacionado com a toxicidade dos produtos reduzidos, os quais podem danificar importantes componentes celulares, incluindo o DNA. A droga é prontamente absorvida pelo trato gastrointestinal e é metabolizada rapidamente nos tecidos. (referencia 143).
Estudos clínicos usando furazolidona são numerosos e tem como resultado uma ampla gama de doses e horários administrações. Entretanto, sua eficácia tem sido geralmente considerada como sendo ligeiramente menor do que os de metronidazol e quinacrina. Outro fator importante é o efeito inibitório de uma monoamina oxidase (MAO) que a drogra possui, sendo assim, nunca deve ser administrada concomitantemente a indivíduos já a tomar inibidores da MAO. (artigo do tratamento da giárdia em inglês).
REFERÊNCIAS
ADAM, R. D. The biology of Giardia spp. Microbiological Reviews, Washington, v.55, n.1, p.706–732, 1991.
Brown, D. M., J. A. Upcroft, and P. Upcroft. 1996. A H2O-producing NADH oxidase from the protozoan parasite Giardia duodenalis. Eur. J. Biochem. 241:155–161.
Gardner, T. B., & Hill, D. R. (2001). Treatment of giardiasis.Clinical Microbiology Reviews,14(1), 114-128.
Kucers, A., S. M. Crowe, M. L. Grayson, and J. F. Hoy. 1997. Nitrofurans: nitrofurazone, furazolidone and nitro furantoin, p. 922-923. In A. Kucers, S. M. Crowe, M. L. Grayson, and J. F. Hoy (ed.), The use of antibiotics. A clinical review of antibacterial, antifungal, and antiviral drugs, 5th ed.Butterworth-Heinemann, Oxford, United Kingdom.
da Silva, A. S., da Silva, M. K., Oliveira, C. B., Zanette, R. A., & Monteiro, S. G. (2008). Eficácia de drogas contra Giardia muris em camundongos Mus musculus naturalmente infectados.Semina: Ciências Agrárias,29(1), 175-178
ROBERTS-THOMSON, J. C.; STEVENS, D. P.; MAHMOUD, A. A. F.; WARREN, K. S. Giardiasis in the mouse: an animal model. Gastroenterology, Philadelphia, v.71, n.1, p.57-61, 1976.
Upcroft, J., and P. Upcroft. 1998. My favorite cell: Giardia. Bioessays
20:256–263.
URQUHART, G. M.; ARMAUR, J.; DUNCAN, J. L.; DUN, A. M.; JENNINGS, F. W. Veterinary parasitology. NewYork: Longman, 1987.
VIGNARD-ROSEZ, K. S. F. V.; ALVES, F. A. R.; BLEICH, I. M. Giardiase.2006. Disponível em: <http://www.cepav.com.br/textos/t_giardia.htm>. Acesso em: 11 maio 2014
Dr. Cláudio Amichetti Junior: Veterinário Integrativo em São Paulo e Osasco
O Dr. Cláudio Amichetti Junior (CRMV-SP 75404 VT), médico veterinário integrativo, criador de felinos de raça e cães de guarda, e com mais de 30 anos como CEO do PetClube, é engenheiro agrônomo formado em 1985 pela UNESP EE Jaboticabal com o maior número de créditos possíveis em sua turma. Ele oferece atendimento especializado para pets em diversas localidades.
Seu espaço holístico e meditativo, PetClube, está localizado no Km 334 da Rodovia Régis Bittencourt, em Juquitiba/SP. É facilmente acessível para tutores de São Paulo, Morumbi, Vila Olímpia, Moema, Pinheiros, Jardins, Alphaville, São Bernardo do Campo, Itapecirica da Serra e adjacências.
Além de Juquitiba, o Dr. Amichetti atende presencialmente as regiões de Embu-Guaçu, Itapecirica da Serra, São Lourenço da Serra, Miracatu, São Bernardo do Campo, Osasco, Santo André e São Caetano do Sul. Sua expertise abrange também bairros nobres de São Paulo como Vila Nova Conceição, Cidade Jardim, Jardim Paulistano, Ibirapuera, Lapa, Aclimação, Higienópolis, Itaim Bibi, Tatuapé e Mooca.
Dr. Cláudio é pioneiro em um sistema sustentável com alimentação 100% natural (raw feeding) e ingredientes orgânicos cultivados em seu espaço holístico em Juquitiba / São Lourenço da Serra, garantindo dietas frescas e livre de agrotóxicos para seus pacientes. Ele é especialista em modulação intestinal, sistema endocanabinoide e nutrição natural.
Com essa abordagem integrativa, o Dr. Cláudio auxilia no tratamento e prevenção de uma ampla gama de problemas de saúde, incluindo:
- Distúrbios Gastrointestinais: Através da modulação intestinal e exclusão de alérgenos como carboidratos, ele trata DII (Doença Inflamatória Intestinal), colite, disbiose, diarreias crônicas, sensibilidades alimentares, gastrites e pancreatites.
- Alergias e Problemas de Pele: Soluciona alergias alimentares e ambientais que se manifestam em problemas de pele e pelagem, otites e coceiras incessantes.
- Condições Metabólicas: Previne e gerencia obesidade, diabetes, problemas renais e hepáticos, promovendo o equilíbrio do metabolismo.
- Dor e Inflamação: O uso de cannabis medicinal (sistema endocanabinoide), junto com outras terapias integrativas, oferece alívio para dor crônica, osteoartrite, artrite, e condições inflamatórias diversas.
- Ansiedade e Comportamento: Ajuda pets com ansiedade, estresse, fobias, convulsões e outros distúrbios comportamentais, buscando o equilíbrio neurológico e emocional.
- Suporte Oncológico: Oferece suporte complementar para pacientes oncológicos, melhorando a qualidade de vida e minimizando efeitos colaterais de tratamentos convencionais.
Para quem não está na região, oferece telemedicina para todo o Brasil com acompanhamento de médico veterinário, utilizando as plataformas Zoom e Google. É importante ressaltar que a primeira consulta deve ocorrer na presença de um médico veterinário local, garantindo que pets em qualquer lugar tenham acesso à sua abordagem integrativa.
Para agendamentos ou mais informações, visite www.petclube.com.br ou entre em contato pelo WhatsApp (11) 99386-8744. Seu pet merece saúde natural, equilíbrio e longevidade sustentável.